-
경영정보 ㅣ 정책법률
인보사 여파, 세포·유전자치료제 허가절차 강화
식약처, 유전학 계통분석 제출 의무화 등 고시안 행정예고
- 기사입력2019-06-07 11:19
이창호 기자 (xg139@junggi.co.kr) 다른기사보기
-
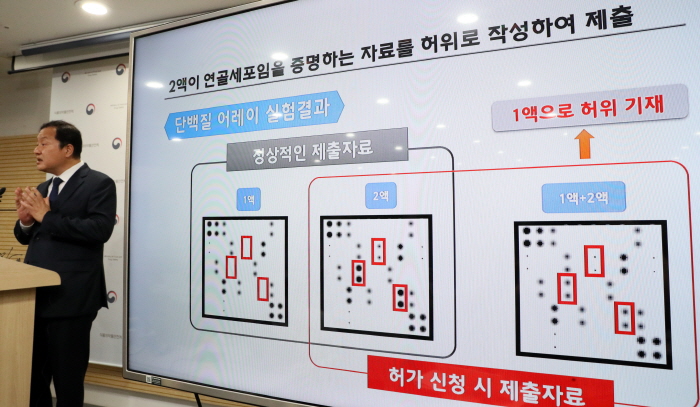
인보사 사태의 재발을 막기 위해 세포·유전자치료제의 허가절차가 강화된다.
식품의약품안전처는 세포·유전자치료제의 허가 신청 시 유전학적 계통 분석(STR 등) 결과 제출을 의무화하는 것을 주요 내용으로 하는 ‘생물학적제제 등의 품목허가·심사 규정’ 일부개정고시(안)을 행정예고 한다고 7일 밝혔다. STR(Short Tandom Repeat)은 DNA의 비교·분석을 통해 같은 계통의 세포임을 확인하는 검사다.고시안의 주요 개정사항을 보면, ▲세포·유전자치료제의 세포은행 구축·운영과정에서 세포의 일관성을 확인할 수 있는 유전자 계통 분석결과 제출 ▲첨부용제가 있는 의약품은 제조방법에 용기의 규격 기재 ▲혈액제제 제조방법 기재 요령 제공 등이다.
식약처는 이번 행정예고에 대해 “최근 유전자치료제의 주성분 세포가 허가사항과 다른 것으로 확인됨에 따라 최초 제품개발 당시와 최종 생산제품의 일관성을 확인하기 위해 추진한 것”이라고 설명했다.
앞서 식약처는 코오롱생명과학의 골관절염 유전자치료제인 인보사케이주에 대해 허가를 취소했다. 코오롱생명과학은 허가 당시 인보사케이주의 주성분세포를 연골세포로 기재했다. 하지만 실제 주성분세포는 신장세포인 것으로 뒤늦게 밝혀졌다.식약처는 이번 개정안을 통해 세포·유전자치료제의 안전 확보를 바탕으로 국제 경쟁력을 높이는 계기가 될 것으로 기대하며, 앞으로도 품질이 확보된 안전한 의약품을 국민에게 공급할 수 있도록 지속적으로 노력하겠다고 밝혔다. 개정안에 대한 의견은 8월6일까지 식약처 바이오의약품정책과에 제출할 수 있다. 중기이코노미 이창호 기자
<저작권자 ⓒ 중기이코노미. 무단전재 및 재배포 금지>
- 관련기사 ㅣ 허위자료 제출, 코오롱 인보사 허가취소·형사고발
- 관련기사 ㅣ “코오롱 인보사…국회 청문회 열어 사실규명을”
- 관련기사 ㅣ 환자단체 “인보사 사태, 감사원 감사 실시해야”